Hormesis y adaptación celular:
impulsores del rendimiento, salud y recuperación
La capacidad del cuerpo humano para adaptarse a situaciones difíciles es una de las claves de nuestra supervivencia como especie. Cada vez que nos enfrentamos al frío o al calor, al esfuerzo físico, al ayuno o a determinados compuestos naturales de los alimentos, el organismo pone en marcha mecanismos internos de protección y ajuste. Estas respuestas no buscan evitar el estrés, sino aprender a gestionarlo de forma más eficiente a nivel celular y mitocondrial.
Estos estímulos reciben el nombre de estresores horméticos: desafíos de baja o moderada intensidad que activan rutas celulares adaptativas y fortalecen la resiliencia biológica. Entre ellos se incluyen el ejercicio, la restricción energética, las variaciones térmicas y los fitoquímicos vegetales.
Todos estos estímulos convergen en una vía central de regulación celular: NRF2. El proceso es común:
- El organismo percibe un desafío controlado,
- NRF2 se activa,
- Se refuerzan los sistemas de defensa, limpieza y reparación celular.
En el estilo de vida moderno —caracterizado por comodidad constante, sedentarismo, estrés crónico y dietas pobres en compuestos bioactivos— estos sistemas se activan cada vez menos. Como consecuencia, el organismo pierde parte de su capacidad natural de respuesta. En este contexto, la reintroducción consciente de estresores horméticos emerge como una estrategia fisiológica para restaurar mecanismos ancestrales de adaptación y mejorar la salud global.
Este artículo establece el marco conceptual y molecular de la hormesis y de la vía NRF2. En publicaciones posteriores se desarrollará de forma individual cada estresor hormético —ejercicio, ayuno, frío, calor y fitoquímicos— analizando sus mecanismos específicos, aplicaciones prácticas y evidencia científica.
Proteína NRF2: función molecular y regulación
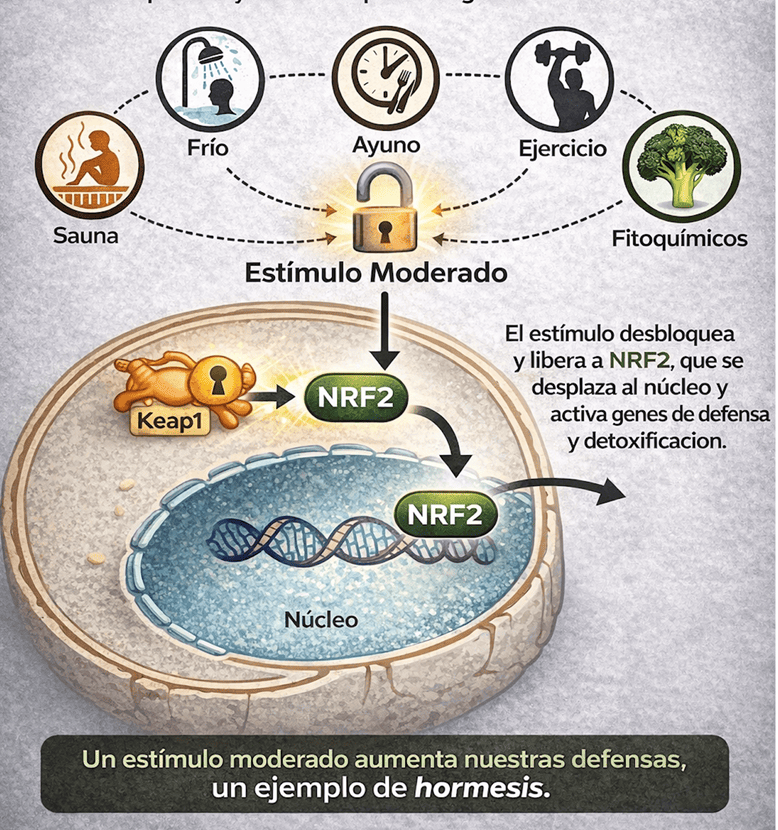
NRF2 es una proteína que activa los sistemas de defensa de la célula frente al estrés oxidativo y los procesos de detoxificación. En condiciones basales, la proteína Keap1 mantiene a NRF2 “apagada” en el citoplasma y favorece que se degrade, evitando una activación innecesaria de los sistemas defensivos.
Cuando aparece un estímulo hormético —como el frío, el ayuno, el ejercicio o ciertos compuestos naturales de las plantas— Keap1 deja de bloquearla, libera a NRF2 y ésta se desplaza al núcleo. Allí activa genes que ayudan a neutralizar radicales libres, reparar el daño y mejorar la detoxificación celular, creando un entorno favorable para una función mitocondrial más eficiente.
Este proceso ejemplifica el principio de la hormesis a nivel molecular.
Enzimas reguladas por NRF2 y su impacto mitocondrial
NRF2 coordina grupos de enzimas que funcionan como unidades especializadas de protección frente a radicales libres.
♦ Enzimas antioxidantes clásicas
Son proteínas especializadas que desactivan radicales libres y subproductos oxidativos para evitar daño celular:
- Superóxido dismutasa (SOD)
- Catalasa (CAT)
- Quinona oxidoreductasa 1 (NQO1)
Estas enzimas constituyen la primera línea de defensa frente al aumento transitorio de ROS (moléculas oxidativas) inducido por estímulos adaptativos, protegiendo la integridad funcional de la mitocondria.
♦ Sistema del glutatión: defensa mitocondrial principal
Es el antioxidante maestro de la célula, con un papel especialmente relevante en la mitocondria. Actúa como un auténtico escudo molecular, manteniendo el equilibrio oxidativo, facilitando la eliminación de toxinas y preservando la integridad de la cadena respiratoria, condición necesaria para una producción eficiente de ATP
- Glutatión S-transferasa (GST)
- Glutatión peroxidasa (GPx)
- Glutatión reductasa (GR)
♦ Conexión con la biogénesis mitocondrial
La activación de los sistemas antioxidantes regulados por NRF2 no sólo protege a la célula frente al daño oxidativo, sino que crea un entorno intracelular favorable para la adaptación metabólica y la optimización de la función mitocondrial.
En este contexto, la defensa antioxidante y la detoxificación celular se integran con mecanismos que regulan la cantidad, la calidad y la eficiencia de las mitocondrias. Entre estos mecanismos destaca la activación de programas de biogénesis mitocondrial que permiten a la célula responder de forma más eficiente a incrementos sostenidos en la demanda energética.
Esta transición desde la protección hacia la optimización energética está regulada por proteínas clave del metabolismo celular, entre las que destaca PGC-1α
PGC-1α: regulador central del metabolismo energético y la adaptación mitocondrial
PGC-1α puede entenderse como un interruptor central que regula cómo la célula produce y gestiona su energía. Cuando el organismo se enfrenta a una mayor demanda energética o a un estímulo de estrés fisiológico, esta proteína se activa para ayudar a la célula a adaptarse.
Su función principal es poner en marcha programas que aumentan la capacidad energética celular, estimulando la formación de nuevas mitocondrias y mejorando el rendimiento de las ya existentes. Gracias a ello, la célula no sólo es capaz de generar más energía, sino que lo hace de forma más eficiente y con menor desgaste metabólico, facilitando la adaptación a diferentes situaciones de estrés.
A diferencia de otras proteínas que actúan uniéndose directamente al ADN, PGC-1α funciona como un “director de orquesta”. No da las órdenes por sí sola, sino que coordina la actividad de distintas proteínas reguladoras para que trabajen de forma conjunta.
Gracias a este papel coordinador, PGC-1α es capaz de integrar información sobre el estado energético de la célula, el equilibrio oxidativo y las necesidades metabólicas del momento, transformando todas estas señales en una respuesta adaptativa organizada y eficaz.
Entre sus principales funciones destacan:
- Estimulación de la biogénesis mitocondrial,
- Mejora de la capacidad oxidativa y del metabolismo aeróbico,
- Regulación del metabolismo de lípidos y glucosa,
- Optimización de la eficiencia energética celular.
♦ PGC-1α y biogénesis mitocondrial
PGC-1α pone en marcha programas que permiten a la célula mejorar su capacidad para producir energía, estimulando la creación de nuevas mitocondrias y mejorando el funcionamiento de las existentes.
Este proceso no consiste únicamente en tener “más mitocondrias”, sino en que éstas trabajen mejor. PGC-1α favorece una organización más eficiente de los sistemas internos que generan energía, lo que permite producir ATP de forma más eficaz y con un menor desgaste celular.
La biogénesis mitocondrial inducida por PGC-1α es especialmente importante en tejidos con alta demanda energética, como el músculo esquelético, el corazón o el sistema nervioso.
♦ Interacción funcional entre NRF2 y PGC-1α
NRF2 y PGC-1α actúan de forma coordinada como un sistema integrado de adaptación metabólica. Cada uno cumple una función diferente, pero complementaria.
NRF2 refuerza los sistemas de defensa de la célula, activando mecanismos antioxidantes y de detoxificación que protegen a la mitocondria. PGC-1α se encarga de mejorar la capacidad energética celular, haciendo que las mitocondrias funcionen de forma más eficiente y se renueven con mayor calidad.
Esta cooperación permite una adaptación equilibrada:
- NRF2 protege la mitocondria,
- PGC-1α optimiza su rendimiento y su capacidad funcional.
El resultado es una mitocondria más eficiente, más resistente al estrés y con una mayor flexibilidad metabólica.
♦ PGC-1α como integrador de señales horméticas
PGC-1α responde a diferentes señales que indican a la célula que necesita adaptarse, como cambios en la disponibilidad de energía o la exposición a estímulos de estrés fisiológico. En este sentido, actúa como un sensor e integrador central de la adaptación metabólica.
Cuando estas señales aparecen, PGC-1α traduce la información en cambios estructurales y funcionales sostenidos, mejorando la capacidad energética de la célula a medio y largo plazo. No se trata de una respuesta puntual, sino de una adaptación que aumenta la eficiencia del sistema.
Desde una perspectiva evolutiva, PGC-1α puede entenderse como un mecanismo de optimización energética: ante un entorno desafiante, la célula no sólo activa sistemas defensivos, sino que mejora su maquinaria energética para afrontar futuros retos con mayor eficiencia y con un menor coste oxidativo.
Hormesis: marco integrador de la adaptación celular
La hormesis describe la situación en la que el estrés leve genera adaptación positiva. NRF2 actúa como mediador central de este proceso.
♦ Mecanismo hormético general
Diversos estresares fisiológicos, producen pequeñas cantidades controladas de ROS, que actúan como señales de activación celular. Lejos de ser perjudiciales, estas señales inducen respuestas coordinadas que incluyen::
- Activación de NRF2,
- Refuerzo de los sistemas antioxidantes,
- Optimización de la maquinaria mitocondrial y del metabolismo energético (PGC-1α).
♦ El entorno moderno: estrés sin hormesis
Muchos factores actuales provocan oxidación elevada sin activación hormética adecuada:
- Sueño insuficiente → déficit de melatonina,
- Disfunción mitocondrial → déficit de CoQ10,
- Dieta pobre en fitoquímicos → menor señalización adaptativa (menor activación de las defensas celulares),
- Sedentarismo → ausencia de hormesis fisiológica.
El resultado es estrés oxidativo crónico, inflamación de bajo grado y pérdida de resiliencia celular, acompañada de una menor capacidad de renovación y eficiencia mitocondrial. La reintroducción sistemática de estresores horméticos permite restaurar esta señalización adaptativa perdida.
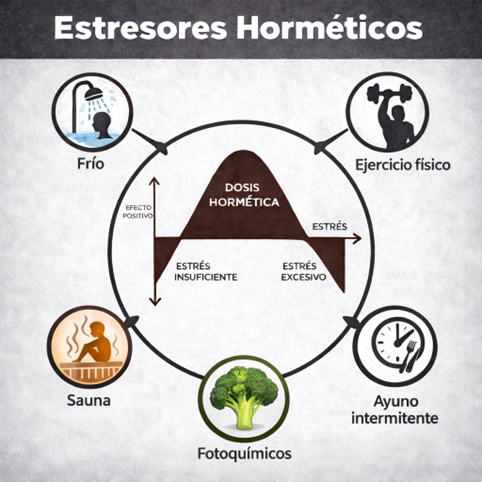
Estresores horméticos ambientales y fisiológicos
Ejercicio físico, ayuno, variaciones térmicas y fitoquímicos dietéticos comparten mecanismos comunes de activación adaptativa, entre ellos la vía NRF2 y la mejora de la función mitocondrial.
El análisis específico de cada uno de estos estresores se desarrollará de forma individual
NRF2 actúa como un nodo central que integra nutrición, estímulos ambientales y estado energético celular. La activación controlada mediante estresores horméticos fortalece las defensas antioxidantes, mejora la función mitocondrial y aumenta la resiliencia metabólica.
La hormesis constituye un principio fisiológico sólido y respaldado por la evidencia científica para preservar la salud celular en un entorno que ha reducido al mínimo los desafíos necesarios para mantenerla

J.R.Celada (Col 56.782)
Referencias científicas
- Cascales Angosto, M. (2005). Estrés oxidativo: envejecimiento y enfermedad. Editorial Complutense.
- Know, L. (2018). Mitochondria and the future of medicine. Chelsea Green Publishing.
- Martínez Sánchez, G. (2018). Estrés oxidativo y enfermedades. Editorial Ciencias Mé
- Panacea Editorial. (2022). Hormesis: Recupera tu potencial ancestral. Editorial Panacea.
- Valenzuela, A. (2023). Activa tus mitocondrias: El secreto para una vida más longeva. Alienta Editorial.
- Surh, Y. J. (Ed.). (2016). NRF2 and its modulation in inflammation. Academic Press.